von Dr. Sandro Lorenz
Statistik und Sichtungsnachweis dieser Seite findet sich am Artikelende
| [1.] Slo/Fragment 019 01 - Diskussion Zuletzt bearbeitet: 2014-07-17 19:57:54 Hindemith | Fragment, Gesichtet, SMWFragment, Schurek 2007, Schutzlevel sysop, Slo, Verschleierung |
|
|
| Untersuchte Arbeit: Seite: 19, Zeilen: 1ff (komplett) |
Quelle: Schurek 2007 Seite(n): 9, Zeilen: 7ff |
|---|---|
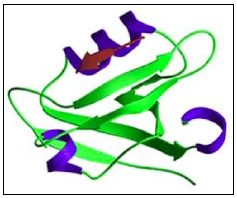
Abb. 1.9: Dreidimensionale schematische Darstellung einer PDZ-Domäne (http://pawsonlab.mshri.on.ca/). 1.3 Das Protein PATJ Die ursprünglich entdeckte Proteinsequenz der murinen Variante von PATJ, CIPP (channel interacting PDZ domain protein), (Kurschner et al., 1998), beinhaltet vier so genannte PDZ-Domänen. Inzwischen ist bekannt, dass es sich bei der von Kurschner et al. 1998 gefundenen Sequenz um eine Verkürzungsmutante handelt und CIPP wie PATJ zehn PDZ-Domänen beinhaltet. PDZ-Domänen (DHRs, discs-large homology regions; GLGF repeats, Gly-Leu-Gly-Phe) sind Protein-Protein-Interaktionsmodule, die in der Sequenz von Gerüstproteinen vermehrt anzutreffen sind. Der Name dieser ca. 90 Aminosäuren langen Module leitet sich von Mitgliedern der MAGUK-Proteinfamilie ab, in denen sie erstmals beschrieben wurden: PSD-95 (postsynaptic density 95)/DLG (discs-large)/ZO- 1 (Ponting, 1997; Saras & Heldin, 1996). Die meisten der bisher bekannten Bindungsmotive von PDZ-Domänen bestehen aus den letzten vier C-terminalen Aminosäuren des Interaktionspartners, wobei Aminosäurereste bis hin zu Position -8 die Bindung beeinflussen können (Hung & Cheng, 2002; Kozlov et al., 2000; Niethammer et al., 1998; Songyang et al., 1997). Inzwischen sind auch interne Bindungsmotive von PDZ-Domänen bekannt (Penkert et al., 2004). Aufgrund der unterschiedlichen Bindungsspezifität wurden PDZ-Domänen in drei Gruppen klassifiziert (Vgl. Tab. 1.3) (Hung & Cheng, 2002). Tab. 1.3: Klassifizierung der PDZ-Domänen anhand der Konsensusbindungssequenz. AS: Aminosäure, X: unspezifische AS, Ф: hydrophobe AS (V, L, I) |
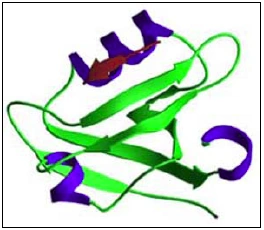
Abb. 1.9: Dreidimensionale schematische Darstellung einer PDZ-Domäne (http://pawsonlab.mshri.on.ca/). 1.5 Das Protein PATJ Die ursprünglich entdeckte Proteinsequenz der murinen Variante von PATJ, CIPP (Channel interacting PDZ domain protein, [46], beinhaltet vier so genannte PDZ-Domänen (Vgl. Abb. 1.9). Inzwischen ist bekannt, dass es sich bei der von Kurschner et al. 1998 gefundenen Sequenz um eine Verkürzungsmutante handelt und CIPP wie PATJ zehn PDZ-Domänen beinhaltet. PDZ-Domänen (DHRs, Discs-large homology regions; GLGF repeats, Gly-Leu-Gly-Phe) sind Protein-Protein-Interaktionsmodule, die in der Struktur von Gerüstproteinen vermehrt anzutreffen sind. Der Name dieser ca. 90 Aminosäuren beinhaltenden Module setzt sich aus Mitgliedern der MAGUK-Proteinfamilie zusammen, in denen diese erstmals beschrieben wurden: PSD-95 [Postsynaptic density]/DLG [Discslarge]/ ZO-1 [70;85]. Die meisten der bisher bekannten Bindungsmotive von PDZ-Domänen bestehen aus den letzten 4 C-terminalen Aminosäuren des Interaktionspartners, wobei Aminosäurereste bis hin zu Position -8 die Bindung beeinflussen können [32;43;63;95]. Inzwischen sind auch interne Bindungsmotive von PDZ-Domänen bekannt [69]. Aufgrund der unterschiedlichen Bindungsspezifität wurden PDZ-Domänen in drei Gruppen klassifiziert (Vgl. Tab. 1.1) [32]. Tab.1.1: Klassifizierung der PDZ-Domänen anhand der Konsensusbindungssequenz. AS: Aminosäure, X: unspezifische AS, Ф: hydrophobe AS (V, L, I) 32. Hung AY, Sheng M: PDZ domains: structural modules for protein complex assembly. J Biol Chem 2002;277:5699-5702. 43. Kozlov G, Gehring K, Ekiel I: Solution structure of the PDZ2 domain from human phosphatase hPTP1E and its interactions with C-terminal peptides from the Fas receptor. Biochemistry 2000;39:2572-2580. 46. Kurschner C, Mermelstein PG, Holden WT, Surmeier DJ: CIPP, a novel multivalent PDZ domain protein, selectively interacts with Kir4.0 family members, NMDA receptor subunits, neurexins, and neuroligins. Mol Cell Neurosci 1998;11:161-172. 63. Niethammer M, Valtschanoff JG, Kapoor TM, Allison DW, Weinberg RJ, Craig AM, Sheng M: CRIPT, a novel postsynaptic protein that binds to the third PDZ domain of PSD-95/SAP90. Neuron 1998;20:693-707. 69. Penkert RR, DiVittorio HM, Prehoda KE: Internal recognition through PDZ domain plasticity in the Par-6-Pals1 complex. Nat Struct Mol Biol 2004;11:1122-1127. 70. Ponting CP: Evidence for PDZ domains in bacteria, yeast, and plants. Protein Sci 1997;6:464-468. 85. Saras J, Heldin CH: PDZ domains bind carboxy-terminal sequences of target proteins. Trends Biochem Sci 1996;21:455-458. 95. Songyang Z, Fanning AS, Fu C, Xu J, Marfatia SM, Chishti AH, Crompton A, Chan AC, Anderson JM, Cantley LC: Recognition of unique carboxyl-terminal motifs by distinct PDZ domains. Science 1997;275:73-77. |
Ein Verweis auf die Quelle fehlt. |
|
Letzte Bearbeitung dieser Seite: durch Benutzer:Hindemith, Zeitstempel: 20140519210948

