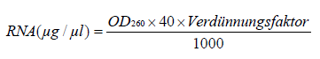von Dr. Florian Freese
Statistik und Sichtungsnachweis dieser Seite findet sich am Artikelende
| [1.] Flf/Fragment 031 01 - Diskussion Zuletzt bearbeitet: 2014-08-18 01:24:50 Graf Isolan | Flf, Fragment, Freese 2010, Gesichtet, SMWFragment, Schutzlevel sysop, Verschleierung |
|
|
| Untersuchte Arbeit: Seite: 31, Zeilen: 1ff (komplett) |
Quelle: Freese 2010 Seite(n): 38, 39, Zeilen: 38: 8ff; 39: 1-7 |
|---|---|
| 3.2.2.3 Gelelektrophorese und optische Konzentrationsmessung (Photometrie)
Zur Kontrolle der Qualität der Proben und der Ermittlung des RNA-Gehalts und der Reinheit wurden diese in einer Gelelektrophorese bei 90 Volt aufgetragen und fotografiert. RNA lässt sich deutlich an zwei spezifischen Banden der ribosomalen 28S- und der 18S-RNA (rRNA) erkennen und von Verunreinigungen unterscheiden. Abbildung 3: Nachweis der extrahierten RNA mittels Gelelektrophorese. Abb. 3: Elektrophorese mit den rRNA-spezifischen Banden der 28S und der 18S-Untereinheit. Waren die Banden in allen Proben gut zu identifizieren, wurde anschließend die genaue RNA-Konzentration mit dem Photometer bestimmt. Dazu wurden 4μl der RNA mit 96μl DEPC versetzt und nach vorheriger Leerkontrolle wurde die Dichte der Probe bei 260 (A1) und bei 280 (A2) nm Wellenlänge gemessen. Zur optimalen Qualität der Probe sollte der Quotient A1/A2 zwischen 1,5 und 2 liegen, da sonst von einer Proteinverunreinigung oder einer Degradation der RNA ausgegangen werden musste. Die Konzentration wurde nach dem Lambert-Beerschen Gesetz berechnet. Die errechnete Konzentration stellte die Grundlage für die weiteren quantitativen Analysen mittels Taqman-PCR dar. |
3.2.2.3 Gelelektrophorese und optische Konzentrationmessung (Photometrie)
Zur Validierung der Qualität der Proben und der Ermittlung des RNA-Gehalts und der Reinheit wurden diese in einer Gelelektrophorese bei 90 Volt aufgetragen und fotografiert. RNA lässt sich deutlich an zwei spezifischen Banden der 28S- und der 18S-Einheit erkennen und von Verunreinigungen unterscheiden. Abbildung 3: Nachweis der extrahierten RNA mittels Gelelektrophorese. Sichtbar sind die mRNA-spezifischen Banden der 28S und der 18S-Untereinheiten. Waren die Banden in allen Proben gut zu identifizieren, so wurde anschließend die genaue RNA-Konzentration mittels Photometrie gemessen. Dazu wurden 4μl der RNA mit 96μl DEPC versetzt und nach vorheriger Leerkontrolle wurde die Dichte der Probe [Seite 39] bei 260 (A1) und bei 280 (A2) nm Wellenlänge im Photometer gemessen. Zur optimalen Qualität der Probe sollte der Quotient A1/A2 zwischen 1,5 und 2 liegen, da sonst von einer Proteinverunreinigung oder einer Degradation der RNA ausgegangen werden musste. Die Konzentration wurde nach dem Lambert-Beerschen Gesetz berechnet. Die errechnete Konzentration stellte die Grundlage für weitere quantitative Analysen mittels Taqman-PCR dar. |
Ein Verweis auf die Quelle fehlt. |
|
Letzte Bearbeitung dieser Seite: durch Benutzer:Graf Isolan, Zeitstempel: 20140818012606