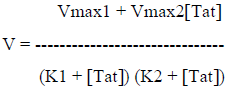|
|
| Untersuchte Arbeit: Seite: 27, Zeilen: 1-12 |
Quelle: Huang 2002 Seite(n): 17, 18, Zeilen: 17: letzter Absatz; 18: 1ff |
|---|---|
| 0,1 μg 20S Proteasom wurden mit 10, 5, 2,5, 1,25, 0,625, 0,3125, 0,15625 und 0 μM/ml Tatpeptide 1, 2 und 5 30 min bei 37°C vorinkubiert. Anschließend wurde das Peptidsubstrat zugegeben und die Fluoreszenz mit dem „Fluostar STL“ bei RT gemessen.
Die Daten wurden nach folgender Formel analysiert: Dabei wurden für das Tat-Protein und den 11S Regulator zwei Bindungsstellungen am 20S Proteasom angenommen. Die Bedeutungen der kinetischen Konstanten Vmax1, Vmax2, K1 und K2 sind durch folgende Gleichungen erklärt: |
0,1 μg 20S Proteasom wurden mit 10, 5, 2,5, 1,25, 0,625, 0,3125, 0,15625 und 0 μM/ml Tatpeptide 1, 2 und 5 30 min bei 37°C vorinkubiert. Anschließend wurde das Peptidsubstrat zugegeben und die Fluoreszenz mit dem „Fluostar STL“ bei RT gemessen.
[Seite 18] Die Daten wurden nach folgender Formel analysiert: Dabei wurden für das Tat-Protein und den 11S Regulator zwei Bindungsstellungen am 20S Proteasom angenommen. Die Bedeutungen der kinetischen Konstanten Vmax1, Vmax2, K1 und K2 sind durch folgende Gleichungen erklärt: |
Ein Verweis auf die Quelle fehlt. Beide Arbeiten verwenden ein Vmax, das nirgendwo definiert ist. |
|